Nuestro objetivo principal es realizar simulaciones biomoleculares de algunos de los procesos que, de forma cooperativa, intervienen en la inflamación, con el fin de conseguir una visión muy detallada de sus mecanismos, y así avanzar en el diseño racional de métodos . y fármacos que permitan controlar la inflamación con lo menos posible de efectos secundarios indeseables para la salud humana.
Hemos dividido el proyecto en varios apartados, compartiendo todos ellos la característica de aplicar la Química Teórica al estudio de diversos aspectos de los procesos inflamatorios.
Lipoxigenasas y La Inflamación
Las lipoxigenasas (LOX) forman una familia de enzimas peroxidantes de lípidos que se han implicado en una serie de procesos fisiológicos y en la patogénesis de enfermedades inflamatorias, hiperproliferativas y neurodegenerativas. La reacción LOX constituye un tipo especial de peroxidación lipídica y se diferencia de las reacciones no enzimáticas en diversos aspectos, como una mayor velocidad de reacción, una selectividad limitada del sustrato, mecanismos de interferencia reguladora y la alta especificidad del producto. La peroxidación lipídica no enzimática convierte a un sustrato determinado en una compleja serie de productos primarios de oxigenación, mientras que los LOX suelen generar un solo isómero de producto.
Durante los últimos años nuestro grupo ha estado estudiando el mecanismo catalítico de diversas isoformas de LOX (conejo ALOX15, cerdo ALOX15, coral ALOX15b, ALOX5) con ácidos linoleico y araquidónico como sustrato mediante cálculos de Docking, Molecular Dynamics y QM/MM. Estos estudios han revelado el origen molecular de la exquisita regioespecificidad de la catálisis LOX que conduce a la formación de agentes inflamatorios o antiinflamatorios. Actualmente nuestro principal objetivo es ALOX5, el LOX humano más importante, que cataliza la hidroperoxidación del ácido araquidónico que conduce ya sea a los agentes proinflamatorios conocidos como leucotrienos o, en combinación con ALOX15, que conduce a la formación de lipoxinas, moléculas antiinflamatorias. . Además, nos centraremos en la proteína activadora de la 5-lipoxigenasa (FLAP).
Efectos Alostéricos de la 15-LOX
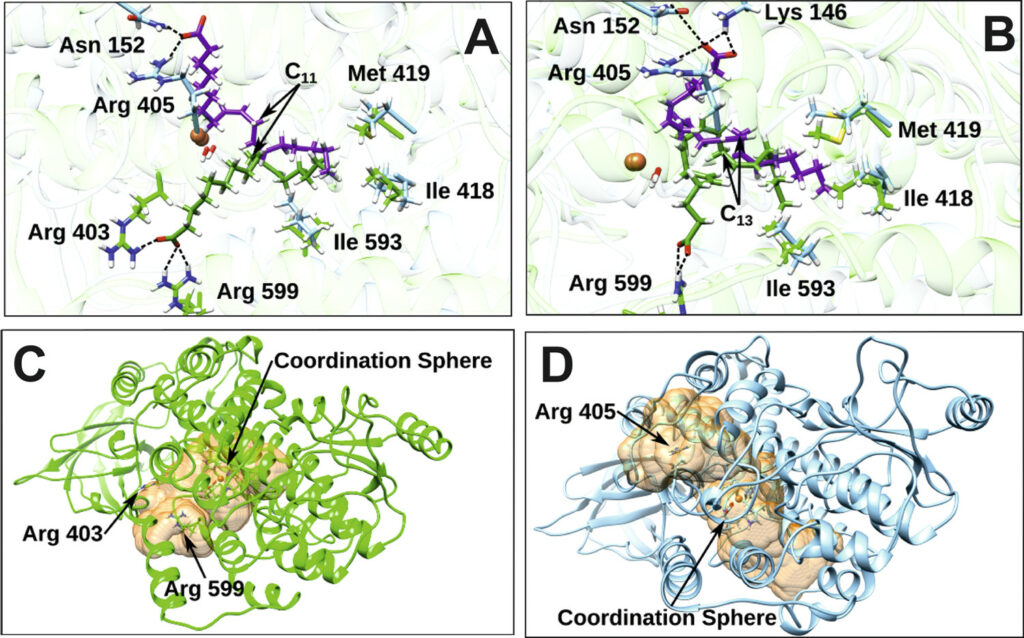
Las lipoxigenasas (LOX) forman una familia de enzimas peroxidantes de lípidos que se han implicado en una serie de procesos fisiológicos y en la patogénesis de enfermedades inflamatorias, hiperproliferativas y neurodegenerativas. La reacción LOX constituye un tipo especial de peroxidación lipídica y se diferencia de las reacciones no enzimáticas en diversos aspectos, como una mayor velocidad de reacción, una selectividad limitada del sustrato, mecanismos de interferencia reguladora y la alta especificidad del producto. La peroxidación lipídica no enzimática convierte a un sustrato determinado en una compleja serie de productos primarios de oxigenación, mientras que los LOX suelen generar un solo isómero de producto.
Durante los últimos años nuestro grupo ha estado estudiando el mecanismo catalítico de diversas isoformas de LOX (conejo ALOX15, cerdo ALOX15, coral ALOX15b, ALOX5) con ácidos linoleico y araquidónico como sustrato mediante cálculos de Docking, Molecular Dynamics y QM/MM. Estos estudios han revelado el origen molecular de la exquisita regioespecificidad de la catálisis LOX que conduce a la formación de agentes inflamatorios o antiinflamatorios. Actualmente nuestro principal objetivo es ALOX5, el LOX humano más importante, que cataliza la hidroperoxidación del ácido araquidónico que conduce ya sea a los agentes proinflamatorios conocidos como leucotrienos o, en combinación con ALOX15, que conduce a la formación de lipoxinas, moléculas antiinflamatorias. . Además, nos centraremos en la proteína activadora de la 5-lipoxigenasa (FLAP).
Ciclooxigenasas i La Inflamación
La prostaglandina endoperóxido H sintasa (PGHS), también conocida como ciclooxigenasa (COX), es una enzima bifuncional con actividades ciclooxigenasa y peroxidasa que convierte el ácido araquidónico (AA) en prostaglandinas (PG). Existen dos isoformas de COX, COX-1 y COX-2, y su actividad se ve afectada por el tratamiento con aspirina. Mientras que la COX-1 acetilada no produce ningún producto oxidado, la COX-2 bloquea la generación de PG y mantiene la producción de 11R- y 15-HETE, metabolitos con actividad pro-resolutiva que tienen implicaciones terapéuticas para la inflamación.
El mecanismo exacto que impone la estereoespecificidad en la oxigenación de ácido araquidónico por parte de la COX-2 y los cambios inducidos por el tratamiento con aspirina no se han aclarado completamente. El objetivo actual de los investigadores es utilizar cálculos de Dinámica Molecular y QM/MM para comprender mejor estos procesos y diseñar nuevos inhibidores, como fotointerruptores con propiedades específicas de inhibición de la COX-2 para cada isómero
Diseño de Biocatalizadores
Los estudios se centran en entender los mecanismos del metabolismo de los leucotrienos proinflamatorios y diseñar enzimas mutadas que puedan producir mediadores antiinflamatorios. Concretamente, los estudios investigan la conversión del leucotrieno A4 en dihidroxi leucotrieno B4 por la leucotrieno A4 hidrolasa humana (LTA4H) y la síntesis de compuestos antiinflamatorios de maresina a partir de intermedios epóxidos mediante el uso de enzimas LTA4H y LOX mudos. Se utilizan métodos computacionales para diseñar y probar enzimas mutadas, con las secuencias de nucleótidos resultantes compartidas con colaboradores experimentales para un estudio posterior. El objetivo final es identificar nuevas vías para la producción de mediadores antiinflamatorios y potencialmente desarrollar nuevas intervenciones terapéuticas para enfermedades inflamatorias.