Àngels González Lafont va ser doctora en Ciències Químiques per la Universitat Autònoma de Barcelona (UAB) l’any 1989 i professora d’universitari a la UAB l’any 1992. Catedràtica de Química Física a la UAB des de 2011. Directora de 20 Tesis Doctorals (+1 en curs), inclosa una amb Doctorat Industrial en col·laboració amb una empresa biotecnològica. Publicació de 169 articles científics (+4 en l’àmbit de la docència).
La meva trajectòria científica va començar en el camp de la Química Atmosfèrica. Vaig utilitzar la teoria de l’estat de transició variacional (VTST), incloses les correccions de túnel, per calcular les constants de velocitat dels processos químics significatius de degradació atmosfèrica iniciats pel radical OH. L’any 2003, la meva recerca va evolucionar cap a les simulacions biomoleculars de catàlisi enzimàtica. Vaig començar a utilitzar simulacions clàssiques de Dinàmica Molecular utilitzant un model complet de les biomolècules amb milers d’àtoms i molècules d’aigua per fer càlculs QM/MM per estudiar les superfícies d’energia potencial de diferents mecanismes catalítics que m’han permès tenir un coneixement extens del comportament i la reactivitat de les ciclooxigenases i les lipoxigenases.
Els meus esforços se centren ara en l’ús de tots els meus coneixements teòrics de les lipoxigenases (ALOX5, ALOX15 i ALOX12) i COX-2 juntament amb la meva experiència en metodologies computacionals per modelar sistemes biomoleculars per desenvolupar enfocaments innovadors de Biomedicina Molecular per bloquejar la pro-acció inflamatòria d’aquests enzims i activar la seva funció per resoldre els processos inflamatoris que són la causa subjacent de la majoria de càncers. El disseny racional de nous inhibidors de COX-2 i ALOX5 (la majoria de fàrmacs fotocanviables), el disseny biocatalític de síntesi de MaR1 i en el disseny d’agonistes és el centre de la recerca que faig actualment.
Últimes Publicacions
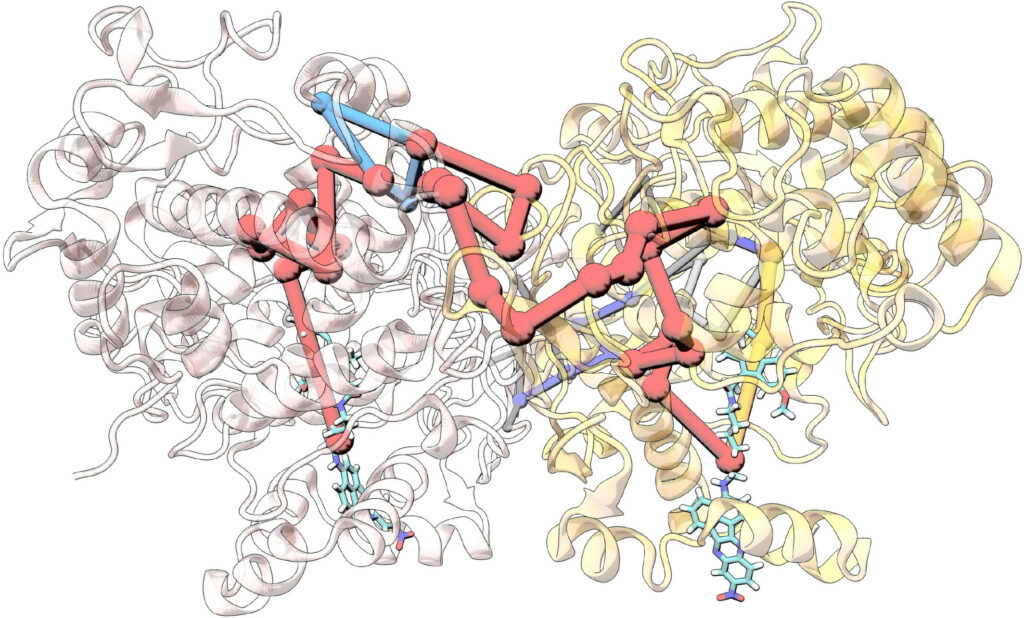
Protein Science
First-principles simulations of the fluorescence modulation of a COX-2-specific fluorogenic probe upon protein dimerization for cancer discrimination
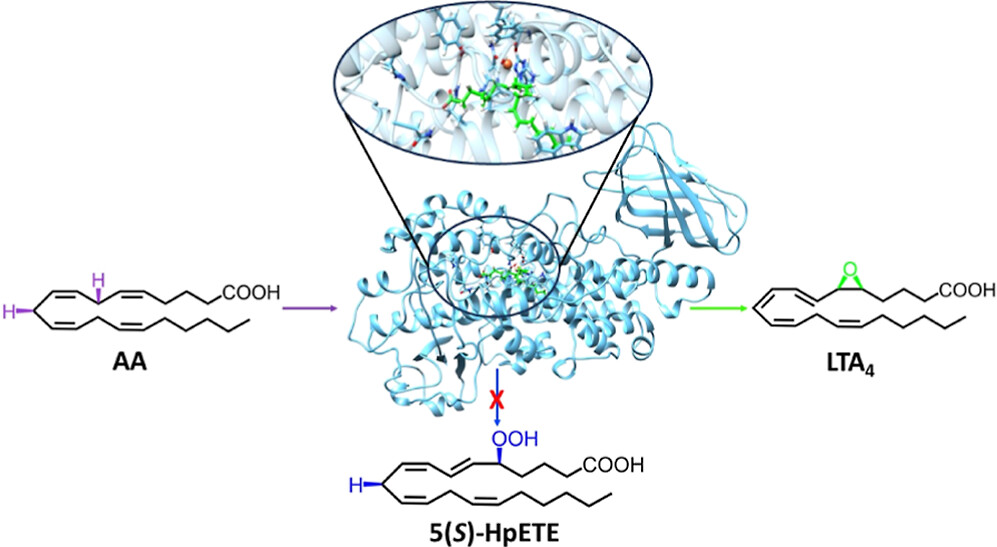
ACS Catalysis
Theoretical Study of the Arachidonic Acid Conversion into Leukotriene A4 Catalyzed by Human 5-Lipoxygenase: Hydroperoxidation and Epoxidation Mechanisms and Arachidonic Acid Active Site Access
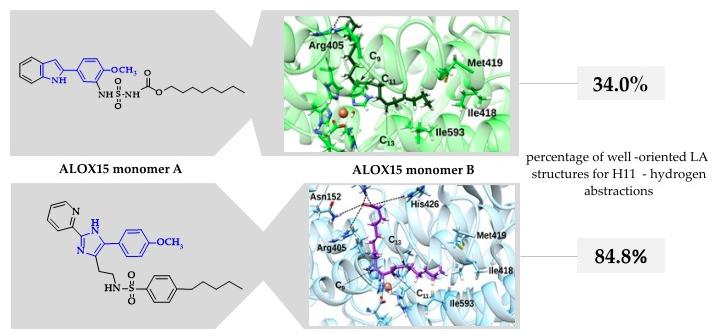
Molecules
Different Structures—Similar Effect: Do Substituted 5-(4-Methoxyphenyl)-1H-indoles and 5-(4-Methoxyphenyl)-1H-imidazoles Represent a Common Pharmacophore for Substrate Selective Inhibition of Linoleate Oxygenase Activity of ALOX15?